


2020-08-12 16:25:32

前 言
本标准按照GB/T 1.1—2009给出的规则起草。
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。
本标准由青岛海关提出、归口并组织实施。
本标准起草单位:青岛海关技术中心、东阿阿胶股份有限公司、中国检验检疫科学研究院。
本标准主要起草人:张晓梅、张鸿伟、张峰、周祥山、田守生、段小波、梁成珠、赵飒、凌云、艾连峰。
本标准系首次发布。
阿胶及含阿胶的食品中动物皮源性成分鉴定方法
1 范围
本标准规定了阿胶及含阿胶的食品中驴皮源性成分、牛皮源性成分、猪皮源性成分、马(骡)皮源性成分的液相色谱-质谱/质谱鉴定方法。
本标准适用于阿胶块、阿胶糕、阿胶膏、阿胶口服液、阿胶浆、阿胶粉、阿胶颗粒等阿胶及含阿胶的食品中动物皮源性成分的鉴定。
2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 6682 分析实验室用水规格和试验方法
3 原理
试样经粉碎后,用1 %碳酸氢铵溶液提取蛋白质,经胰蛋白酶酶解后,采用分子量截留膜过滤获取酶解肽段溶液,液相色谱-质谱/质谱测定皮源性特征肽段。
4 术语和定义
下列术语和定义适用于本文件。
4.1 阿胶
马科动物驴Equus asinus L.的干燥皮或鲜皮经煎煮、浓缩制成的固体胶。
[中华人民共和国药典 2015版 一部,第189页]
5 试剂与材料
除另有规定外,所有试剂均为分析纯,水为符合GB/T 6682规定的一级水。
5.1 试剂
5.1.1 乙腈:色谱纯。
5.1.2 甲酸:色谱纯。
5.1.3 碳酸氢铵:优级纯。
5.1.4 胰蛋白酶:序列分析纯。
5.2 溶液配制
5.2.1 1 %碳酸氢氨溶液:准确称取碳酸氢铵(5.1.3)10.0 g,溶于水并稀释至1 000 mL。
5.2.2 1 mg/mL胰蛋白酶溶液:称取1 mg胰蛋白酶(5.1.4),用1 %碳酸氢铵溶液(5.2.1)1 mL溶解混匀,现用现配。
5.2.3 0.1 %甲酸-水溶液:取甲酸(5.1.2)1 mL,用水稀释至1 000 mL。
5.2.4 0.1 %甲酸-乙腈溶液:取甲酸(5.1.2)1 mL,用乙腈(5.1.1)稀释至1 000 mL。
5.3 对照品、对照标准肽段
5.3.1 对照品:阿胶(对照药材);新阿胶(对照药材);黄明胶(对照药材)。
5.3.2 对照标准肽段:牛皮特征肽A,纯度≥94.0 %;马源寡肽A,纯度≥96.0 %。
5.4 对照品、对照标准肽段溶液制备
5.4.1 1 mg/mL对照品溶液:准确称取10 mg试样,用1 %碳酸氢铵溶液超声处理溶解,再用1 %碳酸氢铵溶液定容至10 mL,摇匀。-20 ℃以下避光保存,有效期6个月。
5.4.2 对照标准肽段溶液:
a) 1 mg/mL对照标准肽段储备液:准确量取1 %碳酸氢氨溶液1 mL溶解1 mg对照标准肽段,溶液浓度为1 mg/mL。-20 ℃以下避光保存,有效期6个月;
b) 0.01 mg/mL对照标准肽段工作液:准确移取对照标准肽段储备液(5.4.2.a)100 μL于10 mL容量瓶中,并用1 %碳酸氢氨溶液稀释至刻度,混匀,-20 ℃以下避光保存,有效期3个月。
5.5 质控样品
5.5.1 质控样品:经过确证分析为相应皮源的阳性样品或阴性样品。
5.5.2 报告限添加样品:
a) 驴皮源报告限添加样品:取经确证为阴性的样品基质0.25 g,超声溶于25 mL的1 %碳酸氢铵溶液中,取100 μL阿胶对照品溶液(5.4.1),用上述样品基质溶液定容至1 mL,该样品溶液相当于非阿胶样品基质中含有1 %(w/w)的阿胶,作为驴皮源性的报告限添加样品;
b) 其他皮源报告限添加样品:取经确证为阴性的样品基质0.25 g,超声溶于25 mL的1 %碳酸氢铵溶液中,分别取100 μL新阿胶、黄明胶对照品溶液(5.4.1),5 μL马源寡肽A标准工作液(5.4.2.b),用上述样品基质溶液定容至1 mL,该样品溶液相当于纯阿胶样品基质中掺入1 %(w/w)的新阿胶和黄明胶及50 ng/mL的马源寡肽A,作为猪皮源性、牛皮源性、马(骡)皮源性的报告限添加样品。
5.6 材料
5.6.1 超滤离心管:2 mL,分子量截留值10 kDa。
5.6.2 滤膜:0.22 μm。
6 仪器和设备
6.1 液相色谱-质谱/质谱分析仪:配有电喷雾离子源(ESI)。
6.2 分析天平:感量为0.01 g和0.000 01 g。
6.3 高速粉碎机。
6.4 超声波仪。
6.5 高速冷冻离心机。
6.6 电热恒温水槽。
7 试样的制备与保存
7.1 试样的制备
取出代表性样品,固体样品冷冻后经粉碎机粉碎,用四分法缩分出不少于5.0 g试样;液体、粉状及颗粒样品均分成两份,每份不少于5.0 g,装入清洁容器内,加封后作出标记,一份作试样,一份作留样。
7.2 试样的保存
按照样品产品标签规定的贮藏条件保存,未标明贮藏条件的,常温避光保存。
8 试验步骤
8.1 提取及净化
8.1.1 阿胶
准确称取0.25 g(±0.01 g)试样,用1 %碳酸氢铵溶液超声溶解,再用1 %碳酸氢铵溶液定容至25 mL。
取上述溶液1.0 mL,过0.22 μm滤膜,精密量取200 μL滤液至2 mL超滤离心管滤膜管中,加胰蛋白酶溶液(1 mg/mL)20 μL,混匀,37 ℃恒温酶解16 h,15 000×g,4 ℃离心10 min,收集下层滤液待上机检测。
8.1.2 含阿胶的食品
准确称取2.5 g(±0.1 g)试样,用1 %碳酸氢铵溶液超声溶解,再用1 %碳酸氢铵溶液定容至刻度25 mL。
将上述溶液12 000×g,4 ℃离心10 min,取上清液1.0 mL,过0.22 μm滤膜,精密量取200 μL滤液至2 mL超滤离心管滤膜管中,加胰蛋白酶溶液(1 mg/mL)20 μL,混匀,37 ℃恒温酶解16 h,15 000×g,4 ℃离心10 min,收集下层滤液待上机检测。
8.1.3 对照品及质控样品
对照品及质控样品按照相应基质(8.1.1或8.1.2)进行提取及净化。
8.2 测定
8.2.1 色谱条件
色谱参考条件:
a) 色谱柱:C18色谱柱(50×2.1 mm,1.3 μm),或相当者;
b) 流动相:A: 0.1 %甲酸-水 B: 0.1 %甲酸-乙腈;
c) 流速:0.3 mL/min;
d) 进样量:10 μL;
e) 柱温:30 ℃;
f) 流动相梯度洗脱程序见表1。
表1 梯度洗脱程序
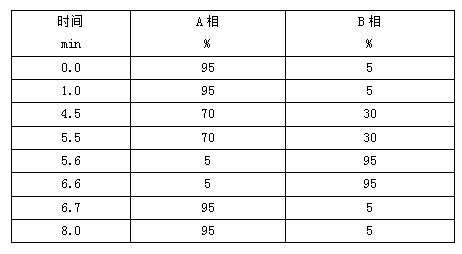
8.2.2 质谱条件
质谱参考条件:
a) 离子源:电喷雾离子源;
b) 扫描方式:正离子扫描;
c) 检测方式:多反应离子监测(MRM);
d) 喷雾电压、碰撞能量、离子源温度等参数应优化至最优灵敏度;
e) 脱溶剂气、碰撞气均为高纯氮气或其他合适气体;
f) 鉴定离子相关参数参见附录A,特征肽段选择离子流色谱图参见附录B。
8.2.3 测定分析序列控制
测定分析序列应当包括对照品溶液、对照标准肽段溶液、测试样品溶液、报告限添加样品溶液、质控样品(程序空白、溶剂空白、阳性质控样或阴性质控样)溶液。
进样顺序按照对照品溶液、对照标准肽段溶液、报告限添加样品溶液、溶剂空白溶液、测试样品溶液、溶剂空白溶液、报告限添加样品溶液、质控样品溶液、溶剂空白溶液、报告限添加样品溶液依次分析。
9 结果判定规则及结果报告
9.1 判定规则
判定规则如下:
a) 试样中各离子对色谱保留时间与相应对照品或对照标准肽段的离子对保留时间相比在±2.5 %的范围内;
b) 阳性质控样品特征肽段相应离子对响应不低于报告限添加样品的相应离子对响应;
c) 测试样品相应皮源的特征肽段的所有离子对响应高于报告限添加样品的相应离子对响应均值;
d) 与对照品或对照标准肽段离子对的离子比率相比,样品中相应离子对的离子比率容许范围为± 30 %。
9.2 结果报告
若同时满足9.1规定的各项判定规则,则判定样品中检出相应皮源性成分;若未同时满足9.1规定的各项判定规则,则判定样品中未检出相应皮源性成分。
10 质量控制
10.1 空白质控样品不得出现各特征肽段的响应。
10.2 阳性质控样品特征肽段相应离子对响应应高于报告限添加样品的相应离子对响应均值。
10.3 报告限添加样品中报告限判定离子对响应的相对标准偏差不超过15 %。
附 录 A
(资料性附录)
各皮源性成分特征肽段鉴定离子对及相关参考参数
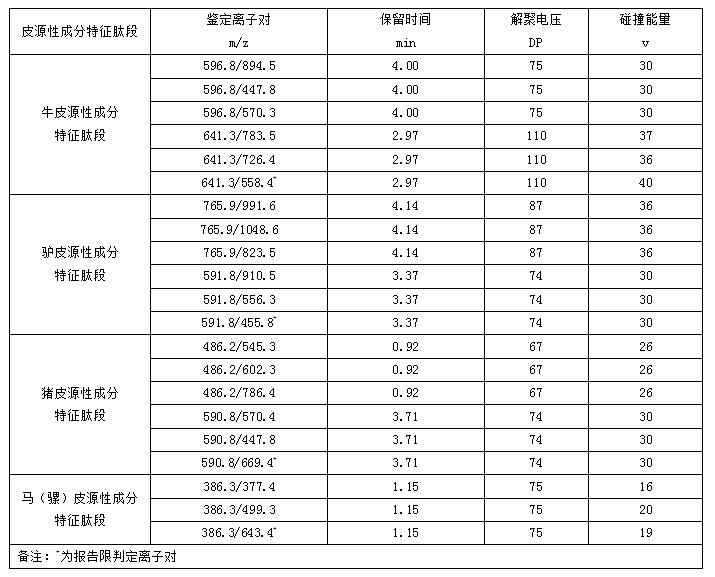
表A.1 各皮源性成分特征肽段鉴定离子对及相关参考参数
附 录 B
(资料性附录)
4种皮源性特征肽段选择离子流色谱图
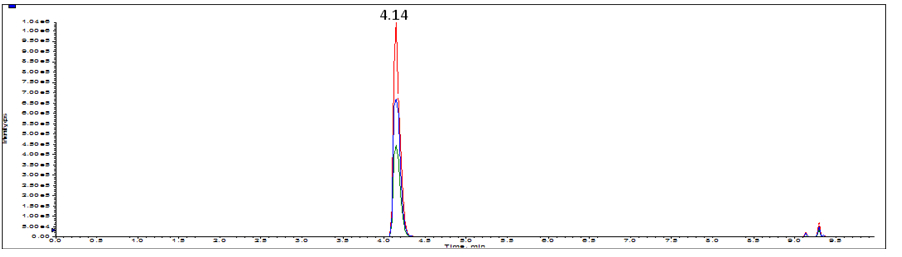
图B.1 驴皮源特征肽(765.9)选择离子流色谱图
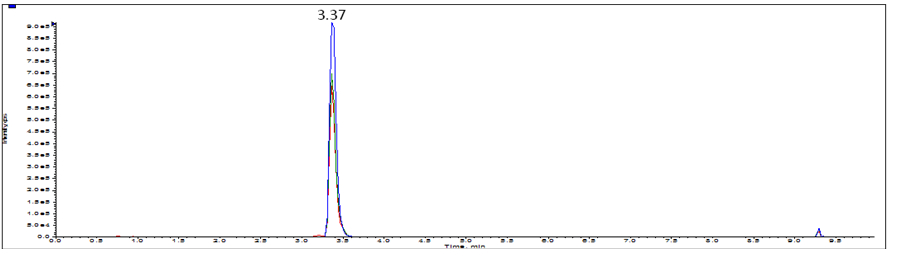
图B.2 驴皮源特征肽(591.8)选择离子流色谱图
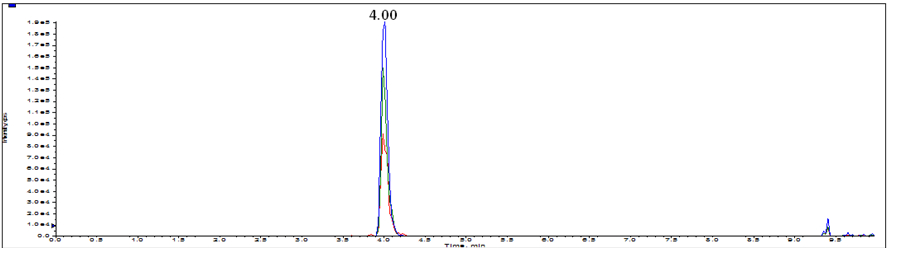
图B.3 牛皮源特征肽(596.8)选择离子流色谱图
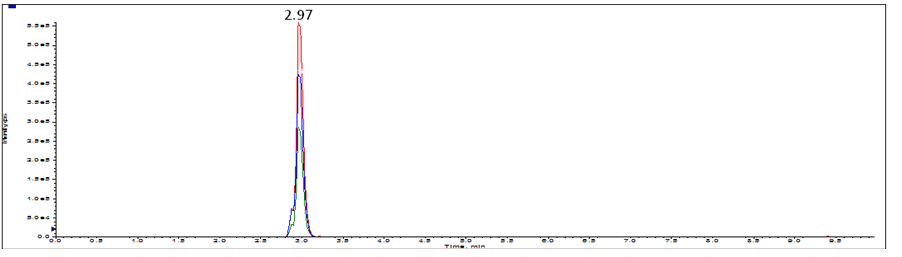
图B.4 牛皮源特征肽(641.3)选择离子流色谱图
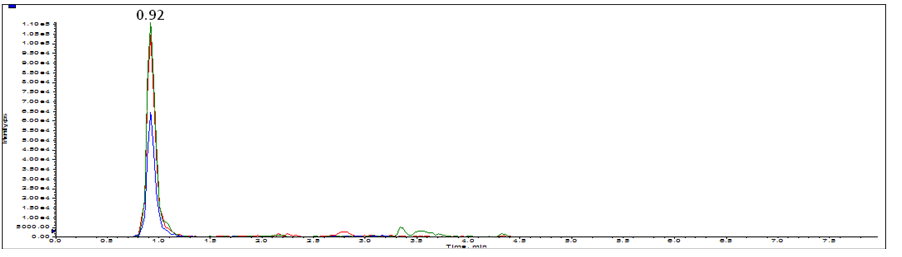
图B.5 猪皮源特征肽(486.2)选择离子流色谱图
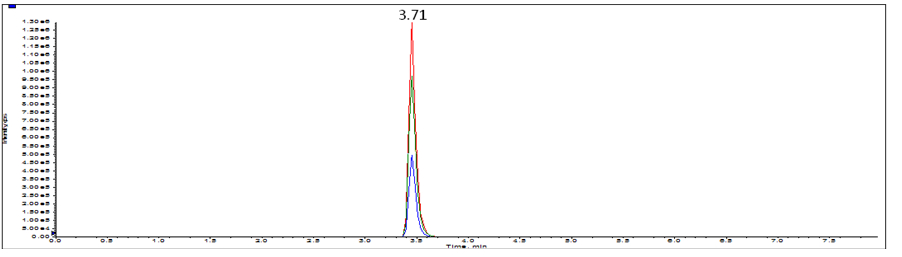
图B.6 猪皮源特征肽(590.8)选择离子流色谱图
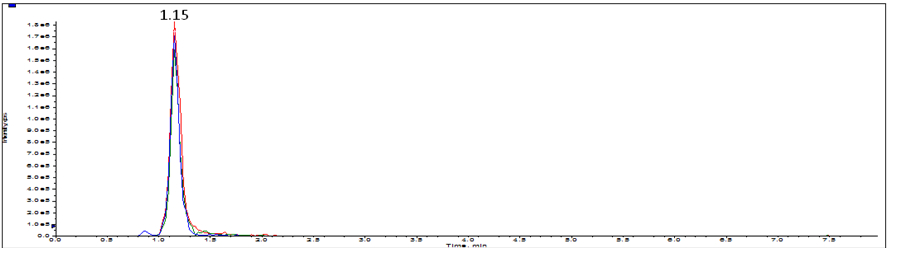
图B.7 马(骡)皮源特征肽(386.3)选择离子流色谱图
上一篇:含阿胶的食品中阿胶含量的测定方法(DB37/T 4010—2020)
下一篇:已经没有了
